بچروت في الكيمياء 2020
- مدّة الامتحان: ثلاث ساعات.
- مبنى النّموذج وتوزيع الدّرجات: في هذا النّموذج فصلان.
الفصل الأوّل – إلزاميّ – 40 درجة
الفصل الثاني – 60 درجة (3×20 درجة)
المجموع – 100 درجة - موادّ مساعدة يُسمح استعمالها:
(1) حاسبة (بما في ذلك الحاسبة البيانيّة)
(2) ملحق قوانين ومعطيات (مُرفق). - تعليمات خاصّة:
- انتبه: في الفصل الأوّل يوجد تسعة أسئلة إلزاميّة.
في كلّ واحد من الأسئلة 1-8 معروضة أربع إجابات، عليك أن וتختار الإجابة الصحيحة منها. عليك الإشارة إلى الإجابات الصحيحة في ورقة الإجابات التي في آخر دفتر الامتحان (صفحة 19).
في السؤال 9 عليكالإجابة عن جميع البنود. - في الفصل الثاني يوجد خمسة أسئلة. عليك الإجابة عن ثلاثة منها.
- انتبه: في الفصل الأوّل يوجد تسعة أسئلة إلزاميّة.
اكتب في دفتر الامتحان فقط. اكتب “مسوّدة” في بداية كلّ صفحة تستعملها مسوّدة.
كتابة أيّة مسوّدة على أوراق خارج دفتر الامتحان قد تسبّب إلغاء الامتحان.
التّعليمات في هذا النّموذج مكتوبة بصيغة المذكّر وموجّهة للممتحَنات وللممتحَنين على حدّ سواء.
نتمنّى لك النّجاح!
الأسئلة
الفصل الأوّل (40 درجة)
أجب عن ثمانية الأسئلة 8-1 (لكلّ سؤال 2.5 درجة).
قبل أن تجيب، اقرأ جميع الإجابات المقترَحة.
لكلّ سؤال مقترَحة أربع إجابات. اختر الإجابة الصحيحة.
- أشر إلى الإجابة التي اخترتَها في ورقة الإجابات التي في الغلاف الداخليّ في آخر دفتر الامتحان (صفحة 19).
- في كلّ سؤال، أشر بقلم حبر بِ X في المربّع الذي تحت الحرف (أ-د) الذي يدلّ على الإجابة التي اخترتَها.
- في كلّ سؤال يجب الإشارة بِ X واحد فقط.
- لمحو إشارة يجب ملء كلّ المربّع على النحو التالي: ■
- يُمنَع المحو بالتيپكس.
- انتبه: يُحبَّذ الامتناع قدر الإمكان عن المحو في ورقة الإجابات، لذلك يوصى أوّلاً بالإشارة إلى الإجابات الصحيحة في نموذج الامتحان نفسه، وبعد ذلك فقط الإشارة إليها في ورقة الإجابات.
- أيّة صيغة تمثيل إلكترونيّة تمثّل صحيحًا جسيمات المركَّب CaCℓ2(s)?
- طاقة التأيُّن الأولى لذرّة الأوكسجين، O ، هي أعلى من طاقة التأيُّن الأولى لذرّة الكبريت، S.
ما هو سبب ذلك؟- في ذرّة الأوكسجين يوجد عدد أقلّ من مستويات الطاقة المسكونة بالإلكترونات بالمقارنة مع ذرّة الكبريت.
- السالبيّة الكهربائيّة لذرّة الأوكسجين أعلى من السالبيّة الكهربائيّة لذرّة الكبريت.
- عدد البروتونات في ذرّة الأوكسجين أصغر من عدد البروتونات في ذرّة الكبريت.
- في الترتيب الدوريّ، يقع الأوكسجين فوق الكبريت.
- معطاة الصِّيَغ الجزيئيّة لأربعة جزيئات: CF4 , CH2FCℓ , CCℓ4 , CH4 .
لجميع الجزيئات مبنى فراغيّ رباعيّ السطوح.
أمامك أربعة أقوال، “أ-د”، تتعلّق بالأربطة التساهميّة )الكوڤلنتيّة( في الجزيء وبقطبيّة الجزيء.
ما هو القول الصحيح؟- في جزيء CF4 جميع الأربطة التساهميّة ليست قطبيّة والجزيء ليس قطبيًّا.
- في جزيء CH4 جميع الأربطة التساهميّة ليست قطبيّة والجزيء قطبيّ.
- في جزيء CCℓ4 جميع الأربطة التساهميّة قطبيّة والجزيء ليس قطبيًّا.
- في جزيء CH2FCℓ جميع الأربطة التساهميّة قطبيّة والجزيء ليس قطبيًّا.
- في الوعاء A يوجد 22 غرامًا من غاز ثاني أكسيد الكربون، CO2(g).
في الوعاء B يوجد 22 غرامًا من غاز الپروپان، C3H8(g).
درجة الحرارة في الوعاءين متساوية، لكنّ الضغط في الوعاء A أقلّ من الضغط في الوعاء B.
ما هو التحديد الصحيح؟- عدد مولات الغاز في الوعاء A أكبر من عدد مولات الغاز في الوعاء B.
- عدد مولات الغاز في الوعاء A أصغر من عدد مولات الغاز في الوعاء B.
- حجم الوعاء A أصغر من حجم الوعاء B.
- حجم الوعاء A أكبر من حجم الوعاء B.
- إلى كأس كيميائيّة (دورق) تحوي 400 ملل من محلول بروميد البوتاسيوم،, KBr(aq)، بتركيز 0.2M، أضافوا 400 ملل من محلول بروميد المغنيسيوم، MgBr2(aq)، بتركيز 0.1M، وخلطوا المحلولين.
أمامك أربعة أقوال IV-I ، تتطرّق إلى المعطيات في الكأس بعد الخلط.- عدد مولات أيونات البروميد، Br‾(aq)، في الكأس هو 0.12 مول.
- عدد مولات أيونات البروميد، Br‾(aq)، في الكأس هو 0.16 مول.
- تركيز أيونات البروميد، Br‾(aq)، في الكأس هو 0.3M.
- ריכוז יוני ברומיד, Br‾(aq)، في الكأس هو 0.2M.
ما هما القولان الصحيحان؟
- القولان I وَ III.
- القولان I وَ IV.
- القولان II وَ IV.
- القولان II وَ III.
- معطاة ثلاثة فلزّات، خارصين Zn(s)، قصدير Sn(s)، أو النحاس Cu(s)، مرتَّبة حسب قدرتها النسبيّة على الاختزال:
Zn(s) > Sn(s) > Cu(s)
في ثلاثة أوعية منفردة C ، B ، A ، معطاة ثلاثة محاليل تحوي، بالإضافة إلى موادّ أخرى، أيونات الفلزّات.
في كلّ واحد من الأوعية يوجد محلول مختلف، كما هو معروضفي الجدول.الوعاء A الوعاء B الوعاء C أيونات موجبة في المحلول أيونات خارصين
Zn2+(aq)
أيونات قصدير
Sn2+(aq)
أيونات نحاس
Cu2+(aq)
أَدخلوا أحد الفلزّات، الخارصين Zn(s)، أو القصدير Sn(s)، أو النحاس Cu(s) إلى أحد الأوعية A أو B أو C.
حدث تفاعل نتج فيه، من ضمن نواتج أخرى، الفلزّ قصدير Sn(s) .
ما هو الفلزّ وما هو المحلول اللذان تفاعَلا؟- فلزّ النحاس، Cu(s)، تفاعَلَ مع المحلول الذي في الوعاء B.
- فلزّ الخارصين، Zn(s)، تفاعَلَ مع المحلول الذي في الوعاء C.
- فلزّ النحاس، Cu(s)، تفاعَلَ مع المحلول الذي في الوعاء A.
- فلزّ الخارصين، Zn(s)، تفاعَلَ مع المحلول الذي في الوعاء B.
- أمامك معادلة تفاعل مثيل أمين، CH3NH2(g)، مع الماء.
CH3NH2(g) + H2O(ℓ) → CH3NH3+(aq) + OH‾(aq)
ما هو التحديد الصحيح؟- في التفاعل المعطى، يتفاعل الماء، H2O(ℓ)، كقاعدة.
- في التفاعل المعطى، يتفاعل مثيل أمين، CH3NH2(g)، كقاعدة.
- في نهاية التفاعل يَنتُج محلول حامضيّ (pH<7).
- في التفاعل، يحدث انتقال إلكترونات من جزيئات مثيل أمين، CH3NH2، إلى جزيئات الماء.
- أمامك مخطّط لتغيّرات إنتالبيا.
ما هي قيمة إنتالبيا التبخير للبروم ؟
|
9. تحليل قطعة من مقال علميّ – إلزاميّ
اقرأ القطعة التي أمامك، وأجب عن جميع البنود “أ – ه” التي تليها (سؤال إلزاميّ – 20 درجة).
خطوة صغيرة على القمر، خطوة كبيرة للكيمياء
المرّة الأولى التي هبط فيها روّاد فضاء على القمر وعادوا إلى الكرة الأرضيّة بسلام، كانت في تاريخ 20 تمّوز 1969
في مهمّة أپولو 11 . ومنذئذ هبطت خمس سفن فضائيّة مع روّاد فضاء على سطح القمر في مهمّة أپولو. وكالة الفضاء
الأمريكيّة ناسا ( NASA ) أعلنت عن نيّتها إرسال روّاد فضاء مرّة أخرى إلى القمر في سنة 2024 .
من أجل الإقلاع من القمر في طريق العودة إلى الكرة الأرضيّة، يجبالتغلّبعلى قوّة جاذبيّة القمر. يستعملون في محرّك
السفينة الفضائيّة وقودًا تلقائيَّ الاشتعالِ (هيپرچوليًّا). الوقود التلقائيُّ الاشتعالِ هو وقود سائليّ يتفاعل فيما بينه في درجة
حرارة الغرفة بالتلامس فقط، دون حاجة للتسخين أو إِحداث شرارة لبدء التفاعل.
في مشروع أپولو كان الوقود التلقائيّ الاشتعال خليطًا سائليًّا من الهيدريزين، N2H4(ℓ)، ومثيل الهيدريزين، NH(CH3)NH2(ℓ)، الذي خُزِن في وعاء معيّن، وَ N2O4(ℓ)، الذي حُفِظ في ضغط عالٍ، في وعاء آخر. عندما تَلامَسَت السوائل، حدث تفاعل فوريّ كَوَّن تيّارًا غازيًّا ملتهبًا في ضغط عالٍ، وهو الذي أدّى إلى إقلاع السفينة الفضائيّة من سطح القمر. عندما أقلعت السفينة الفضائيّة انطلقت شرارات وتكوّنت لهبة على منصّة الإطلاق التي بقيت على أرضالقمر.

أثناء المكوث على القمر، أخذ روّاد الفضاء عيّنات من التربة، استُعملت وما زالت تُستعمَل حتّى اليوم لبحث تركيبتها وعمرها وطريقة تكوُّنها.
الموادّ التي تُركِّب تربة القمر تختلف عن الموادّ الشائعة على سطح الكرة الأرضيّة. مثلاً، على سطح الكرة الأرضيّة تمرّ أيوناتי Fe2+ بأكسدة بواسطة الأوكسجين الذي في الهواء وتتحوّل إلى أيونات Fe3+. هذه العمليّة لا تحدث بتاتًا في القمر، لذلكلا يوجد في تربة القمر مركَّباتتحوي أيونات Fe3+ ، وإنّما مركَّباتتحوي أيونات Fe2+ فقط.
ي عيّنات التربة التي أخذها روّاد الفضاء من القمر، وُجدت أيضًا مركَّبات حَوَت النظير النادر . يتكوّن النظير على سطح القمر في عمليّاتانحلال إشعاعيّ للنظير . من المعلوماتالتي كانتلدى روّاد الفضاء عن النظير ، استنتجوا أنّ القمر تكوّن بعد 60 مليون سنة تقريبًا من تكوُّن المجموعة الشمسيّة.
تخطّط دول عديدة في العالَم مهمّات لبحث القمر. رغم أنّه تجمّعت معلومات كثيرة في أيّامنا عن كيمياء القمر، إ لا لّا لّاأّنّه يُتوقّع ظهور اكتشافات جديدة في هذا الموضوع في المستقبل أيضًا.
المصدر: https://www.chemistryworld.com/2128.tag
- أحد مركِّبات الوقود التلقائيّ الاشتعال هو خليط سائليّ للهيدريزين ومثيل الهيدريزين.
اكتب تمثيلاً كاملاً للصيغة البنائيّة لجزيء الهيدريزين، N2H4، وتمثيلاً كاملاً للصيغة البنائيّة لجزيء مثيل الهيدريزين، NH(CH3)NH2. - حسب القطعة، عندما تتلامس السوائل N2H4(ℓ) وَ NH(CH3)NH2(ℓ) وَ N2O4(ℓ) يحدث تفاعل فوريّ.
לأمامك قولان i وَ ii يتطرّقان إلى التفاعل الذي حدث. حدِّد بالنسبة لكلّ واحد منهما إذا كان صحيحًا أم غير صحيح. علّل كلّ واحد من التحديدين، حسب ما ورد في القطعة.- بالنسبة للتفاعل الذي حدث ΔH0<0.
- طاقة تنشيط التفاعل الذي حدث عالية.
- في تفاعل N2O4(ℓ) مع N2H4(ℓ) ينتج H2O(g) وَ N2(g).
- اكتب معادلة موازَنة للتفاعل.
- في هذا التفاعل، تتفاعل بالكامل 10 كغم N2H4(ℓ). ما هو عدد المولات الكلّيّ للغازات التي تنطلق في التفاعل؟ فصّل حساباتك.
- أيّ مركَّب من مركَّبَي الحديد يمكن إيجاده على سطح القمر: FeS(s)، أم Fe2S3(s)؟
علّل حسب ما ورد في القطعة. - النظير נוצר מן האיזוטופ في مرحلتين متتاليتين لانحلال إشعاعيّ – المرحلة 1 والمرحلة 2.
النظير A هو ناتج في المرحلة 1 ويتفاعل في المرحلة 2 .
- 1. + קרינה רדיואקטיבית מסוג ביתא
קרינה רדיואקטיבית מסוג ____ + .2
- ما هو العدد الذرّيّ للنظير A؟
- ما هو عدد الكتلة للنظير A؟
- ما هو رمز العنصر A؟
- ما هو نوع الأشعّة الإشعاعيّة التي تنطلق في المرحلة 2؟
الفصل الثاني (60 درجة)
أجب عن ثلاثة من الأسئلة 14-10 (لكلّ سؤال 20 درجة).
10. مصطلحات أساسيّة والمبنى والترابط
يتناول السؤال مبنى وصفات مادّتين جزيئيّتين: A وَ B موجوفي وعاءين منفردين.
أمامك جدول يشمل معطيات عن الجزيئيّتين:
| المادّة | درجة حرارة الانصهار (°C) | درجة حرارة الغليان (°C) |
| A | -45 | 157 |
| B | -114 | 78 |
- ما هي الحالة التراكميّة (حالة المادّة) لكلّ واحدة من المادّتين A وَ B في درجة حرارة الغرفة (25°C)؟ علّل.
- أمامك رسمان توضيحيّان يصفان بشكل جزئيّ المبنى الميكروسكوبيّ للمادّتين A ו- B في درجة حرارة الغرفة.

- أمامك أربعة أقوال a-d. بالنسبة لكلّ واحد منها، اذكر إذا كان صحيحًا أم غير صحيح.
- جزيئات المادّتين مركَّبة من نفس أنواع الذرّات.
- المجموعة الويفيّة لجزيئات المادة A يختلف عن عدد ذرّات الكربون في جزيئات المادة B.
- عدد ذرّات الكربون في جزيئات المادة A يختلف عن عدد ذرّات الكربون في جزيئات المادة B.
- في المادّتين A وَ B أشكال حركة الجزيئات هي من نوع اهتزاز (ڤيبريشين) فقط.
- اعتمادًا على التأثيرات المتبادلة التي تعمل بين الجزيئات، حدِّد أيا من الرسمين التوضيحيّ، التوضيحيّ 1 أم الرسم التوضيحي 2، يصف المبنى الميكروسكوبيّ للمادة A. علّل.
- أمامك أربعة أقوال a-d. بالنسبة لكلّ واحد منها، اذكر إذا كان صحيحًا أم غير صحيح.
- إلى كلّ واحد من الوعاءين اللذين توجد فيهما المادّتان A وَ B، أضافوا حجمًا متساويًا من الماء وخلطوا. الرسمان التوضيحيّان 3 وَ 4 يصفان المبنى الميكروسكوبيّ لخليط كلّ واحدة من المادّتين مع الماء بعد الخلط.

الرسم التوضيحيّ 3

الرسم التوضيحيّ 4
- حدِّد أيًّا من الرسمين التوضيحيّين، الرسم التوضيحي 3 أم الرسم التوضيحي 4، يصف محلولاً بطريقة ميكروسكوبيّة؟ علّل تحديدك.
- اكتب معادلة تفاعل الإذابة في الماء للمادّة الملائمة للرسم التوضيحيّ الذي اخترتَه في البند الفرعيّ ״جi”
- فسّر لماذا المادّة الأخرى لا تذوب في الماء. اعتمد في إجابتك على التأثيرات المتبادلة بين الجسيمات.
- ما هو الفرق الماكروسكوبيّ بين الخليطين الموصوفين في الرسمين التوضيحيّين 3 وَ 4؟
11. الأكسدة والاختزال والحسابات الكيميائيّة
إسرائيل هي إحدى أكبر المنتِجات في العالم لعنصر البروم، Br2(ℓ) ومركَّباته.
أمامك التفاعل (1) الذي يتفاعل فيه البروم مع الماء لإنتاج محلول HBrO(aq)، الذي يمكن أن يُستعمَل للتعقيم والتبييض.
(1) Br2(ℓ) + H2O(ℓ) → HBrO(aq) + HBr(g)
- א
- حدِّد هل يتفاعل Br2(ℓ) في التفاعل (1) كمؤكسِد فقط، أم كمختزِل فقط، أم كمؤكسِد وكمختزِل أيضًا. علّل تحديدك.
أدخلوا مادّة مختزِلة إلى محلول HBrO(aq). حَدَثَ تفاعُل.
- حدِّد أيّة أيونات تتواجد في المحلول في نهاية التفاعل: أيونات Br‾(aq) أم أيونات BrO3‾(aq). علّل تحديدك.
أمامك التفاعل (2) الذي تَنتُج فيه أيونات BrO3‾(aq).
(2) 3BrO‾(aq) → 2Br‾(aq) + BrO3‾(aq)
- ב
- كم مول إلكترونات مرّت في التفاعل الذي نَتَجَ فيه 1 مول أيونات BrO3‾(aq)؟ علّل.
أيونات BrO3‾(aq) سامّة. التركيز الأقصى المسموح به لِ BrO3‾(aq) في الماء هو 0.01 ميكروغرام في اللتر.
معطى أنّ: 1 ميكروغرام = 10-6 × 1 غرام.- ما هو العدد الأقصى المسموح به لأيونات BrO3‾(aq) في 1 لتر من الماء؟ فصّل حساباتك.
معطى أنّه: في مول واحد من الجسيمات يوجد 1023×6.02 جسيم.
عنصر البروم هو سامّ وخطِر، لذلك يتمّ حفظه في أوعية خزن مغلقة. في حالة وقوع تسرُّب، يُفاعِلون بخار البروم مع الأمونيا، NH3(g). يحدث التفاعل (3).
(3) 3Br2(g) + 8NH3(g) → N2(g) + 6NH4Br(s)
- ג
- حدِّد هل يتفاعل NH3(g) في التفاعل (3) كمؤكسِد فقط، أم كمختزِل فقط، أم كمؤكسِد وكمختزِل أيضًا.
- كم كيلوغرام NH4Br(s) يَنتُج عندما تتفاعل 8.0 كغم من بخار البروم مع الأمونيا؟ فصّل حساباتك.
- ما هو حجم غاز النيتروجين، N2(g) ،في شروط STP الذي يَنتُج عندما تتفاعل 8.0 كغم من بخار البروم مع الأمونيا؟ فصّل حساباتك.
معطى أنّ: الحجم المولاريّ للغاز في شروط STP هو 22.4 لتر.
12. كيمياء الغذاء
الطحالب غنيّة بمركِّبات غذائيّة كثيرة. تحوي الطحالب جميع الأغذية الأساسيّة وڤيتامينات وأملاحًا معدنيّة كثيرة.
الجدول الذي أمامك يعرضمعطيات لحامضَيْن دهنيَّين حيويّيْن موجودَيْن في الطحالب:
| اسم الحامض الدهنيّ | حامضالأراكيدونيك (ARA) | حامضالإيكوسابنتاينويك (EPA) |
| درجة حرارة الانصهار (ºC) | -49 | -54 |
| تمثيل مختصر للصيغة البنائيّة للجزيء | 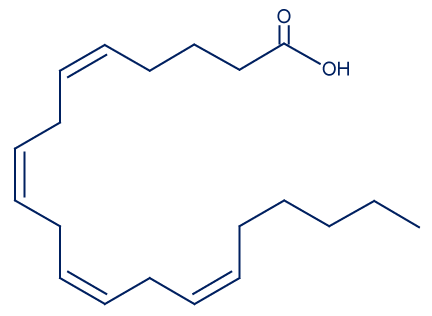 | —————- |
| كتابة مختصرة للحامض الدهنيّ | —————— | C20: 5ω3 cis cis cis cis cis |
- i. ما هي الأحماضالدهنيّة الحيويّة؟
ii. اكتب كتابة مختصرة للحامضالدهنيّ ARA.
iii. اكتب تمثيلاً مختصرًا للصيغة البنائيّة لجزيء الحامضالدهنيّ EPA. - درجة حرارة انصهار حامضالستياريك C18:0، (St) ، هي 69.6°C.
درجة حرارة انصهار حامضالستياريك أعلى بكثير من درجة حرارة انصهار الحامضين الدهنيّين المعطيين، ARA وَ EPA.
فسّر هذا التحديد. اعتمد في إجابتك على التأثيرات المتبادلة التي تعمل بين الجزيئات.
عندما يُنتِجون مُضافًا غذائيًّا من الطحالب، يُحبَّذ إضافة مضادّات أكسدة لمنع أكسدة الأحماضالدهنيّة الحيويّة الموجودة في الطحالب ولحفظها لوقت طويل.
معطاة صيغتان بنائيّتان مختصرتان للڤيتامينَيْن C وَ E اللذين يعملان مضادَّي أكسدة (أنتي أوكسيدينتات):
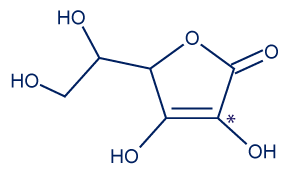 | 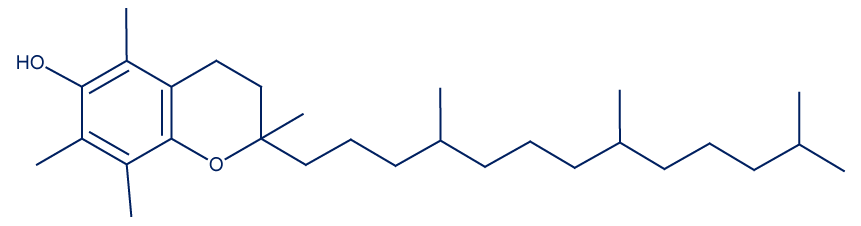 |
| ڤيتامين C | ڤيتامين E |
- ذرّة الكربون المُشار إليها بِ * في الصيغة البنائيّة المختصرة للڤيتامين C تشترك في عمليّة يُستعمَل فيها الڤيتامين مضادّ أكسدة.
- ما هي درجة أكسدة ذرّة الكربون المُشار إليها بِ * في الصيغة البنائيّة المختصرة للڤيتامين C؟
- من بين الأقوال a-c التي أمامك، اذكر ما هي الأقوال التي تلائم وصف نشاط الڤيتامين C كمضادّ أكسدة.
- درجة أكسدة ذرّة الكربون المُشار إليها بِ * ترتفع.
- ڤيتامين C يتفاعل كمؤكسِد في عمليّات الأكسدة – الاختزال.
- ڤيتامين C يمنع عمليّات أكسدة غير مرغوب فيها للموادّ.
- حدِّد أيّ ڤيتامين، C أم E، هو أقلّ ملاءَمة ليُستعمَل مضادّ أكسدة يذوب في خليط الحامضين الدهنيّين المعطيين. فسّر تحديدك.
- أحد الأملاح المعدنيّة الهامّة الموجودة في الطحالب هو المركَّب KI. هذا المركَّب هو مصدر لأيونات اليوديد ‾ I.
לحسب تعليمات وزارة الصحّة، الاستهلاك اليوميّ الموصى به لليود هو 150 ميكروغرام أيونات يوديد.
أوراق الطحالب “نوري” تُستعمَل لتحضير السوشي ومأكولات أخرى. في ورقة طحالب “نوري”، التي وزنها 2.5 غرام، يوجد 45 ميكروغرام أيونات يوديد.
حدِّد هل وجبة الحساء التي حُضِّرت من 10 غرامات من أوراق الطحالب “نوري” تحوي بالضبط كمّيّة أيونات اليوديد الموصى بها في اليوم أم أكبر من الكمّيّة الموصى بها أم أقلّ منها. فصّل حساباتك وفسّر.
13. חומצות ובסיסים
في تجربة أجراها طلّاب في المختبر, أشاروا إلى كأس بالحرف A , وفيها أذابوا في الماء 3.6 غرام من هيدروكسيد الصوديوم الصلب، NaOH(s)..
نتج في الكأس A محلول حجمه 600 ملل.
- i. اكتب معادلة عمليّة الإذابة التي حدثت أثناء تحضير المحلول في الكأس A.
ii. هل pH المحلول في الكأس A أصغر من 7، أم مساوٍ لِ 7 أم أكبر من 7؟ علّل.
قسّم الطلّاب المحلول الذي في الكأس A بشكل متساوٍ إلى ثلاث كؤوس كيميائيّة I، II، III. في كلّ كأس 200 ملل محلول، كما هو موصوف في الرسم التوضيحيّ 1.

- i. أمامك أربعة أقوال a-d، تتطرّق إلى المحاليل التي في الكؤوس I، II، III، كما هو موصوف في الرسم التوضيحي 1.
اذكر ما هي الأقوال الصحيحة من الأقوال a-d.- عدد مولات المادّة المذابة في كلّ واحدة من الكؤوس هو أصغر من عدد مولات المادّ ة المذابة في المحلول الذي كان في الكأس A.
- عدد مولات المادّة المذابة في كلّ واحدة من الكؤوس هو مساوٍ لعدد مولات المادّة المذابة في المحلول الذي كان في الكأس A.
- تركيز المحلول في كلّ واحدة من الكؤوس هو أصغر من تركيز المحلول الذي كان في الكأس A.
- تركيز المحلول في كلّ واحدة من الكؤوس هو مساوٍ لتركيز المحلول الذي كان في الكأس A.
ii. احسب عدد مولات المادّة المذابة في كلّ واحدة من الكؤوس I، II، III. فصّل حساباتك.
- התלמידים הוסיפו לכל אחת מן הכוסות I، II، III תמיסות שונות זו מזו.
לכוס I הוסיפו התלמידים נפח מסוים של תמיסה של חומצת מימן כלורי، HCℓ(aq) ، בריכוז 0.2M، וערבבו היטב. התרחשה תגובה.
בתום התגובה ערך ה- pH היה 7.- נסח ניסוח נטו לתגובה שהתרחשה.
- מהו נפח תמיסת HCℓ(aq) שהוסיפו לכוס I؟ פרט את חישוביך.
לכוס II הוסיפו התלמידים 150 מ”ל תמיסת חומצה גופרתית، H2SO4(aq) ، בריכוז 0.2M، וערבבו היטב. התרחשה תגובה.
- קבע אם בתום התגובה ה- pH בכוס II היה חומצי، בסיסי או ניטרלי.
פרט את חישוביך או נמק באופן מילולי.
- לכוס III הוסיפו התלמידים 80 מ”ל תמיסת אלומיניום כלורי، AℓCℓ3(aq). צבע התמיסה נהפך ללבן עכור.
לפניך ניסוח נטו לתגובה שהתרחשה.Aℓ3+(aq) + 3OH‾(aq) → Aℓ(OH)3(s)
כל המגיבים הגיבו בשלמות.
חשב את ריכוז תמיסת AℓCℓ3(aq) שהוסיפו לכוס III.
14. מבנה וקישור، אנרגייה
שאלה זו עוסקת בחומרים פחמן דו-חמצני، CO2(g) ، ופחמן דו-גופרי، CS2(ℓ).
- i. הסבר מדוע، בטמפרטורת החדר، פחמן דו-גופרי הוא נוזל ואילו פחמן דו-חמצני הוא גז.
בתנאים מתאימים، פחמן דו-חמצני מתמוסס בפחמן דו-גופרי.
- הסבר מדוע פחמן דו-חמצני، CO2(g) ، מתמוסס בפחמן דו-גופרי، CS2(ℓ).
- נסח את תהליך ההמסה של פחמן דו-חמצני בפחמן דו-גופרי.
- i. סרטט את נוסחת הייצוג האלקטרונית של מולקולת CO2 ואת נוסחת הייצוג האלקטרונית של מולקולת CS2.
ii. בטבלה שלפניך נתונים ערכי אנתלפיית הקשר של שני סוגי הקשרים המופיעים במולקולות CO2 ו- CS2.
התאם לכל ערך את סוג הקשר המתאים. ציין את הגורמים להבדל בין אנתלפיות הקשר.אנתלפיית הקשר
kJ⁄moℓ (קג’אול למול)הקשר 803 573 - אנתלפיית האידוי של פחמן דו-גופרי היא 27.6kJ⁄moℓ.
- נסח את התגובה של אידוי פחמן דו-גופרי ורשום את ערכו וסימנו של ΔH0 לתגובה.
נתון ניסוח התגובה של שרפת פחמן דו-גופרי נוזלי (1) וכן שינוי האנתלפייה המלווה את התגובה.
(1) CS2(ℓ) + 3O2(g) → CO2(g) + 2SO2(g) ΔH01=-1076.1 kJ
נתון ניסוח התגובה של שרפת פחמן דו-גופרי גז (2).
(2) CS2(g) + 3O2(g) → CO2(g) + 2SO2(g) ΔH02=؟
- חשב את הערך של ΔH02. פרט את חישוביך.
- בכל מולקולה של גופרית דו-חמצנית، SO2 ، אטום הגופרית קשור לשני אטומי חמצן.
נסמן כל אחד מן הקשרים ב- S–O.
נתון אנתלפיית הקשר של O=O היא 497kJ⁄moℓ.
חשב את ערכה של אנתלפיית הקשר בקשר S–O במולקולת SO2.
היעזר בנתונים שבשאלה، ובתשובותיך בסעיפים הקודמים. פרט את חישוביך.